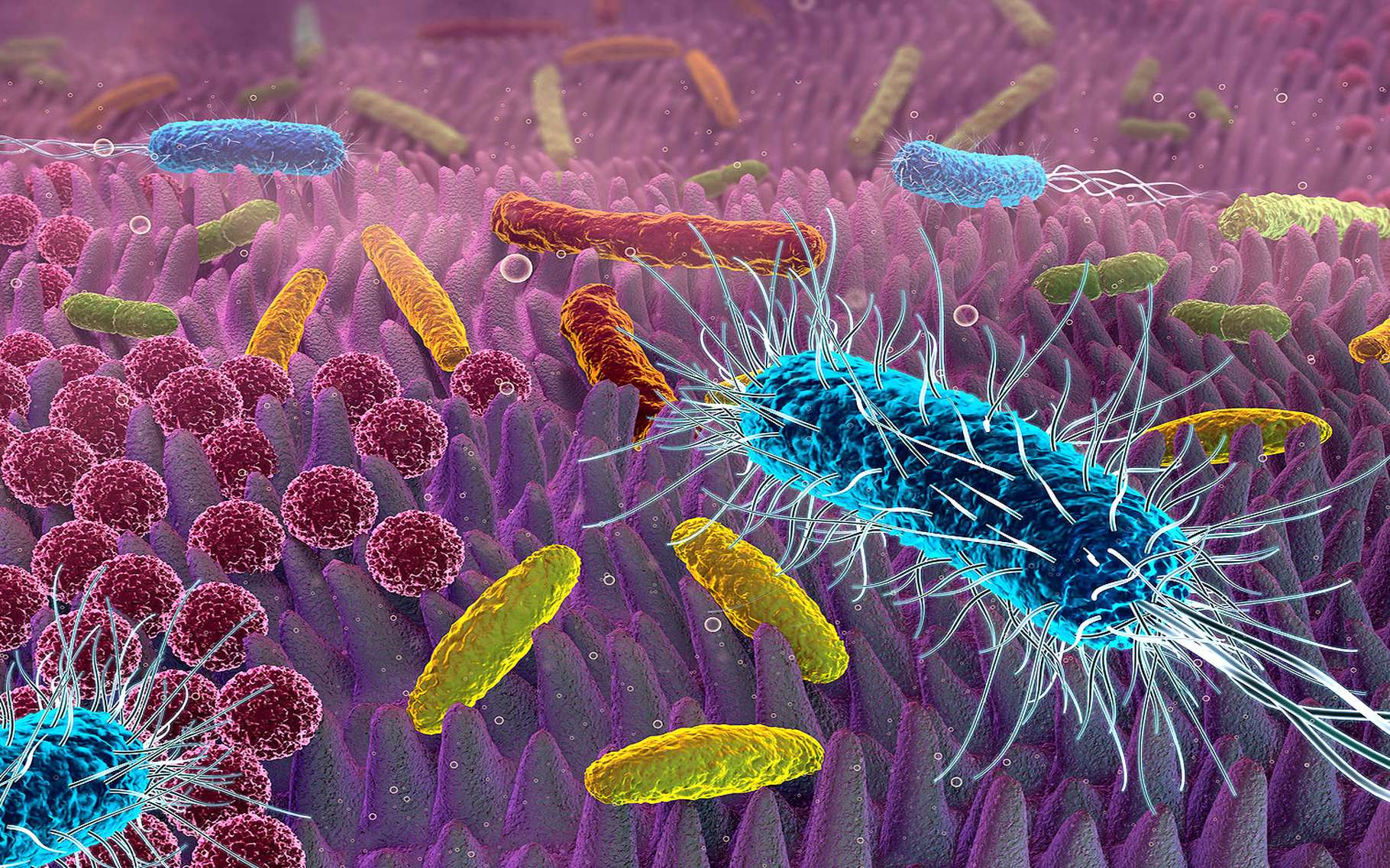
Les sous-produits du microbiote intestinal circulent dans la circulation sanguine et régulent les processus physiologiques de l'hôte, notamment l'immunité, le métabolisme et les fonctions cérébrales. Des scientifiques de l'Institut Pasteur (organisme de recherche partenaire de l'Université Paris Cité), de l'Inserm et du CNRS ont découvert que les neurones hypothalamiques d'un modèle animal détectent directement les variations de l'activité bactérienne et adaptent l'appétit et la température corporelle en conséquence. Ces résultats démontrent qu'il existe un dialogue direct entre le microbiote intestinal et le cerveau, une découverte qui pourrait conduire à de nouvelles approches thérapeutiques pour lutter contre les troubles métaboliques tels que le diabète et l'obésité. La publication de ces résultats dans la revue Science est prévue pour le 15 avril 2022.
L'intestin est le plus grand réservoir de bactéries de l'organisme. Un nombre croissant de données révèle le degré d'interdépendance entre les hôtes et leur microbiote intestinal, et souligne l'importance de l'axe intestin-cerveau. A l'Institut Pasteur, des neurobiologistes de l'Unité Perception et Mémoire (Institut Pasteur/CNRS)[1], des immunobiologistes de l'Unité Microenvironnement et Immunité (Institut Pasteur/Inserm), et des microbiologistes de l'Unité Biologie et Génétique de la Paroi Cellulaire Bactérienne (Institut Pasteur/CNRS/Inserm)[2] ont partagé leur expertise pour étudier comment les bactéries de l'intestin contrôlent directement l'activité de certains neurones du cerveau.
Les scientifiques se sont concentrés sur le récepteur NOD2 (domaine d'oligomérisation des nucléotides) qui se trouve à l'intérieur de la plupart des cellules immunitaires. Ce récepteur détecte la présence de muropeptides, qui sont les éléments constitutifs de la paroi cellulaire des bactéries. De plus, il a été établi précédemment que des variantes du gène codant pour le récepteur NOD2 sont associées à des troubles digestifs, dont la maladie de Crohn, ainsi qu'à des maladies neurologiques et des troubles de l'humeur. Cependant, ces données étaient insuffisantes pour démontrer une relation directe entre l'activité neuronale dans le cerveau et l'activité bactérienne dans l'intestin. C'est ce qu'a révélé le consortium de scientifiques dans cette nouvelle étude.
En utilisant des techniques d'imagerie cérébrale, les scientifiques ont d'abord observé que le récepteur NOD2 chez la souris est exprimé par des neurones dans différentes régions du cerveau, et en particulier dans une région appelée hypothalamus. Ils ont ensuite découvert que l'activité électrique de ces neurones est supprimée lorsqu'ils entrent en contact avec des muropeptides bactériens provenant de l'intestin. "Les muropeptides présents dans l'intestin, le sang et le cerveau sont considérés comme des marqueurs de la prolifération bactérienne", explique Ivo G. Boneca, responsable de l'unité Biologie et génétique de la paroi cellulaire bactérienne à l'Institut Pasteur (CNRS/Inserm). A l'inverse, si le récepteur NOD2 est absent, ces neurones ne sont plus supprimés par les muropeptides. Par conséquent, le cerveau perd le contrôle de la prise alimentaire et de la température corporelle. Les souris prennent du poids et sont plus susceptibles de développer un diabète de type 2, en particulier chez les femelles âgées.
Dans cette étude, les scientifiques ont démontré le fait étonnant que les neurones perçoivent directement les muropeptides bactériens, alors que l'on pensait que cette tâche était principalement confiée aux cellules immunitaires. "Il est extraordinaire de découvrir que des fragments bactériens agissent directement sur un centre cérébral aussi stratégique que l'hypothalamus, connu pour gérer des fonctions vitales comme la température corporelle, la reproduction, la faim et la soif", commente Pierre-Marie Lledo, chercheur au CNRS et responsable de l'unité Perception et Mémoire de l'Institut Pasteur.
Les neurones semblent donc détecter l'activité bactérienne (prolifération et mort) comme un indicateur direct de l'impact de la prise alimentaire sur l'écosystème intestinal. "La consommation excessive d'un aliment spécifique peut stimuler la croissance disproportionnée de certaines bactéries ou pathogènes, mettant ainsi en péril l'équilibre intestinal", explique Gérard Eberl, responsable de l'unité Microenvironnement et immunité de l'Institut Pasteur (Inserm).
L'impact des muropeptides sur les neurones et le métabolisme hypothalamiques soulève des questions sur leur rôle potentiel dans d'autres fonctions cérébrales, et pourrait nous aider à comprendre le lien entre certaines maladies cérébrales et les variants génétiques de NOD2. Cette découverte ouvre la voie à de nouveaux projets interdisciplinaires à la frontière entre les neurosciences, l'immunologie et la microbiologie, et, à terme, à de nouvelles approches thérapeutiques des maladies du cerveau et des troubles métaboliques tels que le diabète et l'obésité.
[1] Cette unité de recherche est également connue sous le nom de "Laboratoire Gènes, Synapses et Cognition" (Institut Pasteur/CNRS). L'Institut du cerveau de Paris (CNRS/Inserm/Sorbonne Université/AP-HP) a également contribué à ces résultats.
[2] Le nom de l'unité du CNRS est "Unité de Microbiologie Intégrative et Moléculaire" et celui de l'unité Inserm est "Unité Interactions Hôte-Microbe et Physiopathologie" (Institut Pasteur/CNRS/Inserm).
Commentaires
Enregistrer un commentaire